So kommt man zu den Covid-Impfschadensfällen der Europäischen Arzneimittelbehörde (EMA)
Der kritische Leser, der mit sich einander widersprechenden Aussagen zu Impfschadensfällen konfrontiert sieht, wird den Wunsch verspüren, sich anhand der ursprünglichen Quellen und Rohdaten eine Meinung bilden zu wollen.
Diese Anleitung soll dabei unterstützen.
Update: 16.12.2021 Die Fallzahlen von BioNTech sind in 2 Kategorien schon am 11.12. nur noch knapp unter 250.000 geblieben und werden sie beim nächsten Update überschreiten. Dann muss weiter aufgeteilt werden! Die BioNTech serious Kategorie in professional und non-professionell. Zusätzlich die BioNTech non-serious non-professional in male und female. Damit werden die BioNTech-Fallmeldungen in insgesamt 6 Einzeldateien heruntergeladen. Wenn das irrsinnig erscheint, seien Sie nachsichtig mit dem Programmierer der Webschnittstelle. Wer konnte ahnen, dass jemals ein Arzneistoff mit nahezu einer Million Schadensmeldungen in einem einzigen Jahr zugelassen wird.
Computertechnologie, das Internet und unzählige Menschen, denen an Aufklärung und Transparenz gelegen ist, erlauben die Bereitstellung einer solchen Menge an Informationen, die noch vor wenigen Dekaden undenkbar gewesen wäre. Eine veröffentlichte Information kommt nicht immer jedem gelegen, und so entbrennt ein Kampf um Transparenz und Deutungshoheit. Der moderne Mensch ist sich aber bewusst, dass Wissen Holschuld ist, und gibt sich nicht mit einfachen Antworten zufrieden. Er will es genau wissen und geht zu den Primärquellen und Rohdaten.
Auch die Webseite EudraVigilance ist vom Wunsch nach Transparenz getragen, und wir können uns glücklich schätzen, dass in den europäischen Behörden trotz des politischen Drucks die Idee der freien Verfügbarkeit von Informationen weiter lebt.
Dass die EudraVigilance die Pharmakovigilanz sämtlicher human- und veterinärmedizinischen Arzneistoffe umfasst, und die Daten automatisiert grafisch aufbereitet werden, geht auf Kosten der Übersichtlichkeit und die verfügbaren Rohdaten sind relativ versteckt. Die Grafiken decken zwar ein weites Spektrum von möglichen Fragen ab, da aber eine ganz entscheidende Information, die Todesfolge, dabei ausgeklammert wurde, geht kein Weg an den Rohdaten vorbei. Der Weg dorthin ist etwas umständlich und ist darum hier auf die minimale Zahl von Eingaben zusammengefasst.
Der beste Zeitpunkt zum Herunterladen ist jeden Samstag 9 Uhr, denn ab 8 Uhr werden neue Daten eingepflegt. Da die Dateien auf 250.000 Zeilen beschränkt sind, muss bei BioNTech und AstraZeneca auf mehrere Dateien aufgeteilt werden. Ich verwende dazu die Kriterien "Seriousness" und "Reporter Group". Zudem muss jahresweise heruntergeladen werden. Die meisten Impfschäden fallen auf 2021, jedoch für BioNTech begannen die Impfungen schon 2020.
- Vorbereitung: den Browser so einstellen, dass im Download-Bereich "Jedes Mal nachfragen, wo eine Datei gespeichert werden soll" ausgewählt ist.
- Aufruf von Pfizer-BioNTech
- Auf den Stichtag der Daten achten. Hier ist zu erkennen, ob die neuen Daten eventuell noch nicht in der Datenbank sind.

- Den Tab "Line Listing" aufrufen
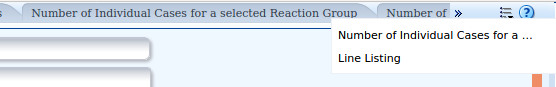
- Bei Seriousness "Select" anklicken
- Die Checkbox "Serious" anklicken
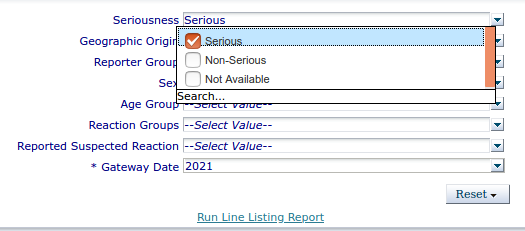
- Bei Reporter group "Select" anklicken und "Healthcare Professional" auswählen
- In den weißen Bereich klicken, so dass die Markierung des Auswahlfeldes "Serious" verschwindet. (Je nach Browser ist die Einstellung sonst nicht übernommen)

- Auf den Link "Run Line Listing Report" klicken
- Ein neues Fenster öffnet sich, das nach einer Zeit eine Tabelle von einigen Fällen enthält.
- Ans Ende der Seite scrollen.
- Link "Export" klicken
- In der Popup-Box auf Data gehen, bis sich eine zweite Popup-Box öffnet.
- In der zweiten Popup-Box auf CSV klicken
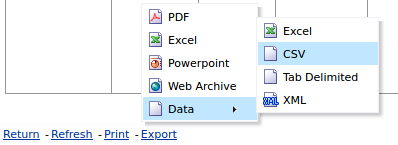
- Nach einer gewissen Zeit öffnet sich ein Popup "The Export process is complete.", den wir ignorieren.
- Je nach Browsereinstellung öffnet sich ein Fenster, das das Herunterladen der Datei ermöglicht. Wir wählen als Dateinamen einen aus, den wir als "BioNTech ernste Schadensfälle von 2021" wiedererkennen können, z.B. B1sp.csv.
- Schließen des Fensters bzw. Tabs "Run Line Listing Report". Es geht weiter im Fenster mit dem Titel "Oracle BI Interactive Dashboards - DAP", dass die Auswahlboxen enthält.
- Klicken auf "Reporter group" und dort "Healthcare Professional" abwählen und "Non Healthcare Professional" und "Not Sepcified" auswählen.
- Ins Weiße klicken und "Run Line Listing Report" anklicken.
- Die obigen Schritte wiederholen und in B1sq.csv speichern.
- Wir klicken ins Fenster Seriousness, wählen die Checkbox "Serious" ab, die Checkboxes "Non-serious" und "Not Available" hingegen aus.
- Im Feld "Reporter Group" wählen wir "Healthcare Professional" aus.
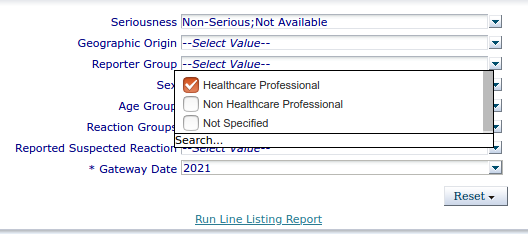
- Ins Weiße klicken und "Run Line Listing Report" anklicken.
- Die obigen Schritte wiederholen, in die Datei B1np.csv speichern, und das "Run Line Listing Report" Fenster wieder schließen.
- Im Feld "Reporter Group" wählen wir "Healthcare Professional" ab, die Felder "Non Healthcare Professional" und "Not Specified" hingegen aus.
- Im Feld "Sex" wählen zusätzlich "Female" aus.
- Die Schritte zum Herunterladen wiederholen und in die Datei B1nqf.csv speichern.
- Im Feld "Sex" "Female" abwählen und "Male" auswählen.
- Die Schritte zum Herunterladen wiederholen und in die Datei B1nqm.csv speichern.
- In den Feldern "Seriousness", "Sex" und "Reporter Group" alle Felder abwählen, so dass dort wieder --Select Value-- steht.
- Das "Gateway Date" 2020 auswählen, ins Weiße klicken, und mit "Run Line Listing Report" die Daten in B0.csv herunterladen.
- Nun geht es weiter mit den Impfschäden von AstraZeneca, die in zwei Teile unterteilt werden müssen.
- Man geht ähnlich vor wie bei BioNTech, muss aber lediglich die "Serious" Fälle in As.csv und die "Non Serious" und "Not Available" Fälle in An.csv speichern.
- Die Fälle von Moderna lassen sich auf die gleiche Weise in einem Rutsch herunterladen, z.B. in die Datei M.csv.
- Genauso lassen sich die Fälle von Janssen-Johnson&Johnson herunterladen, z.B. in die Datei J.csv
Nun hat man die Impfschadensfälle der vier Covid-Impfstoffe in acht Dateien. Die Unterteilung der Dateien könnte auch anders vorgenommen werden, aber jede Datei darf nicht über der 250.000er-Grenze liegen, sonst gehen Daten verloren. Sollten die Fälle weiter steigen, wird auch die Unterteilung noch erweitert werden müssen. Ich wähle das CSV-Format, weil es meinen anfänglichen Tests am robustesten erschien, und in anderen Formaten (außer TSV) Daten fehlten. Das kann sich mit der Weiterentwicklung der Webseite adrreports.eu auch ändern. Die größte Gefahr von Fehlinterpretationen besteht durch den Umstand, dass in der Spalte der Symptome (und auch der Arzneistoffe) mehrere Einträge durch Zeilenende-Zeichen getrennt sind. In der CSV-Datei sind diese Zeilenenden als "<BR><BR> " kodiert, was sich leicht erkennen und umsetzen lässt.
Das Zusammenführen der Dateien und die Weiterverarbeitung der Daten kann auf unterschiedlichen Wegen erfolgen. Ich gebe hier aber allgemeine Hinweise, die für alle Arten der Weiterverarbeitung gelten.
- Fälle, in denen verschiedene Impfstoffe angewendet wurden, treten in der Zusammenführung als Duplikate auf und müssen berücksichtigt werden.
- Die Ernsthaftigkeit (Seriousness) ist Attribut einer Reaktion, nicht eines Falles. Um zu einer Gesamtbewertung des Falles zu kommen, müssen die Attribute des Falles zu einer sinnvollen Gesamtbewertung kombiniert werden. Dieser Umstand unterscheidet sich prinzipiell von der VAERS (US-amerikanische Behörde) und ermöglicht zusätzliche Möglichkeiten der Auswertung.
- Die Tödlichkeit des Falles spiegelt sich im Attribut "Results in Death" eines oder mehrerer Reaktionen wider. Gelegentlich wird auch die Reaktion "Death" geführt. Weil das Attribut mehrfach vorkommen kann, darf man keinesfalls die Zahl der Vorkommen des Suchbegriffs "Results in Death" als Zahl der Todesfälle nehmen (was einigen Analysten offenbar passiert ist).
- Die sehr wichtige Kategorie Behindernd ("Disabling") ist leider nicht feiner aufgeschlüsselt in Umstände, die zu einem Behinderungsgrad im Sinne der Sozialverbände führen oder lediglich zu einer temporären Arbeitsunfähigkeit. Dass es sich bei Disabling prinzipiell um diese beiden Umstände handelt, ergab sich aus einer Analyse von Texten der nationalen Behörden.
- Die Kategorie Krankenhausaufenthalt ("Caused/Prolonged Hospitalisation") bezieht sich sowohl auf Neuaufnahmen ins Krankenhaus als auch auf einen durch die Reaktion verlängerten Krankenhausaufenthalt (der also schon vorher bestand). Eine feinere Aufschlüsslung ist leider nicht möglich.
- Die Daten enthalten leider keine Altersangabe der Person, lediglich eine grobe Klassifizierung in sieben Altersklassen.
- Die Daten enthalten leider keine Landesangabe, lediglich eine Unterteilung in "European Economic Area" und "Non European Economic Area". Großbritannien scheint ab 2021 zur "Non European Economic Area" zu gehören.
- Die Reaktionsbezeichnungen gehören offenbar der MedDRA-Nomenklatur an.
- Neben den eigentlichen Nebenwirkungen finden sich unter den Reaktionen auch Begleitumstände, Untersuchungen, Vorerkrankungen, die sich im Gesamtzusammenhang des Falles erschließen.
- Reaktionen können auch eine Angabe der Dauer tragen, die aber leider relativ selten ausgefüllt wurde.
- Eine Reaktion kann die Angabe tragen, ob sie noch besteht, abgeklungen ist, am abklingen ist, oder ob sie chronisch geworden ist ("Resolved with sequelae"). Leider sind die Angaben nicht konsequent ausgefüllt und man kann nicht von einer generellen Nachbearbeitung des Falls ausgehen, wenn der Betroffene wieder gesund geworden ist.
- Leider findet sich in den Daten (anders als in VAERS) keine Freitextbeschreibung des Falles. So lassen sich der genaue Hergang der Nebenwirkungen und die Begleitumstände nur ungenau aus den Reaktionen ableiten.
- Es gibt leider keine Angabe, ob der Fall von einer der nationalen Behörden eingereicht wurde oder über den Hersteller, was den Abgleich mit den Berichten der nationalen Behörden sehr erschwert.
Das Neueste von Dr. Andreas Hoppe
- EMA-Datenbank – ausführliche Tabellen
- dieKontrollgruppe.de – erste Antworten auf lange gestellte Fragen
- Plötzlich und unerwartet den Impfstoff vergessen
- Erste Ergebnisse von "dieKontrollgruppe.de" belegen: Den Ungeimpften geht's gut!
- Die Kontrollgruppe der offiziellen Studien der Covid-19-"Impfstoffe" wurde aufgelöst – was nun?
